이 콘텐츠는 사이트 회원 전용입니다. 기존의 사용자라면 로그인 하세요. 새 사용자는 아래에서 회원가입 할 수 있습니다.
[보고서] 워드처럼 마음대로 교정 가능한 4세대 유전자가위
- MIT 브로드 연구소와 하버드와 MIT 데이비드 리우 교수...DNA 이중가닥을 자르지 않고, 외부 DNA 주입 없이 마음대로 교정
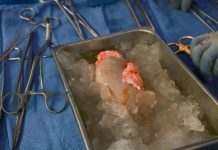
워드프로세서처럼 마음대로 교정할 수 있는 4세대 유전자가위 프라임 에디터(Prime Editor)가 발견돼 현재 전 세계 과학계가 들썩이고 있다. DNA의 이중가닥을 자르지 않고(double-stranded breaks, DSBs) 혹은 외부에서 DNA 주입 없이, 컴퓨터 워드프로세서처럼 누구나 글을 마음대로 쓰고 지울 수 있는, 4세대 유전자 가위인 프라임 교정(Prime Editing), 즉 프라임 에디터(Editor)를 발견했다. 그






















![[보고서] 딥씨크 출현과 한국 AI 미래전략](http://itnews.or.kr/wp-content/uploads/2025/02/7-218x150.png)

![[2024 애플 동향] ③ 애플카 ‘프로젝트 타이탄’의 실패 원인](http://itnews.or.kr/wp-content/uploads/2024/03/1-2-218x150.png)
![[2024 애플 동향] ② 애플카 ‘프로젝트 타이탄’ 10년간 의 여정](http://itnews.or.kr/wp-content/uploads/2024/03/4-218x150.png)
![[2024 애플 동향] ① 애플 프로젝트 타이탄’ 종료](http://itnews.or.kr/wp-content/uploads/2024/03/Midjourney-218x150.png)





